Что такое массовое число атомного ядра? Массовое число численно равно сумме нейтронов и протонов ядра. Его обозначают буквой А. Понятие "массовое число" появилось в связи с тем, что масса ядра обусловлена числом ядерных частиц. Как связаны между собой масса ядра и количество частиц? Давайте выяснять.
Строение атома
Любой атом состоит из ядра и электронов. Кроме атома водорода, так как он имеет всего один электрон. Ядро заряжено положительно. Отрицательный заряд несут электроны. Заряд каждого электрона принят за -1. Атом в целом электронейтрален, то есть не имеет заряда. Это значит, что количество частиц, несущих отрицательный заряд, то есть электронов, равно положительному заряду ядра. Например, в атоме кислорода заряд ядра +8 и электронов 8, в атоме кальция заряд ядра +20, электронов 20.
Строение ядра
 Вам будет интересно:Конструктивная деятельность: виды, цели, методика
Вам будет интересно:Конструктивная деятельность: виды, цели, методика
Ядро состоит из двух видов частиц – протонов и нейтронов. Протоны заряжены положительно, нейтроны не имеют заряда. Таким образом, заряд ядру дают протоны. Заряд каждого протона принят за +1. То есть, сколько протонов содержится в ядре, такой и будет заряд всего ядра. К примеру, в ядре углерода 6 протонов, заряд ядра +6.
В периодической системе элементов Менделеева все элементы расположены в порядке увеличения именно заряда ядра. У водорода заряд ядра +1, он расположен первым; у гелия +2, он второй в таблице; у лития +3, он третий и так далее. То есть заряд ядра соответствует порядковому (атомному) номеру элемента в таблице.
В целом любой атом электронейтрален. Это значит, что количество электронов равно заряду ядра, то есть количеству протонов. А поскольку количество протонов определяет атомный номер элемента, то зная этот атомный номер, мы, таким образом, знаем и количество электронов, и количество протонов, и заряд ядра.
Масса атома
Масса атома (М) определяется массой составных частей, то есть электронов и ядра. Электроны очень легкие по сравнению с ядром и почти не вносят вклада в массу всего атома. То есть масса атома обусловлена массой ядра. Что такое массовое число? Масса ядра определяется числом частиц, входящих в его состав, - протонов и нейтронов. Таким образом, массовое число – это масса ядра, выраженная не в единицах измерения массы (граммы), а в количестве частиц. Конечно, абсолютная масса ядер (m), выраженная в граммах, известна. Но это очень маленькие числа, выражаемые в отрицательных степенях. Например, масса атома углерода m(C) = 1,99 ∙ 10-23 г. Пользоваться такими числами неудобно. И если нет необходимости в абсолютных значениях массы, а нужно просто сравнить массы элементов или частиц, то пользуются относительными массами атомов (Ar), выраженными в а.е.м. Относительная масса атома указана в таблице Менделеева, например, у азота 14,007. Относительная масса атома, округленная до целого числа, и есть массовое число ядра элемента (A). Массовые числа такие, что ими удобно пользоваться – это всегда целые числа: 1, 2, 3 и так далее. Например, у азота – 14, у углерода – 12. Их записывают верхним левым индексом, к примеру, 14N или 12C.
Когда нужно знать массовое число?
Зная массовое число (A) и атомный номер элемента в периодической системе (Z), можно определить число нейтронов. Для этого нужно вычесть из массового числа протоны.
Зная массовое число, можно вычислить массу ядра или всего атома. Поскольку масса ядра обусловлена массой частиц, входящих в его состав, то она равна произведению количества этих частиц и массы этих частиц, то есть произведению массы нейтрона и массового числа. Масса нейтрона равна массе протона, в целом их обозначают как масса нуклона (ядерная частица).
M=A∙mN
К примеру, рассчитаем массу атома алюминия. Как видно из периодической системы элементов Менделеева, относительная атомная масса алюминия равна 26,992. Округлив, получаем массовое число ядра алюминия 27. То есть его ядро состоит из 27 частиц. Масса одной частицы – постоянная величина, равная 1,67 ∙ 10-24 г. Тогда, масса ядра алюминия равна: 27 ∙ 1,67 ∙ 10-24 г = 4,5 ∙ 10-23 г.
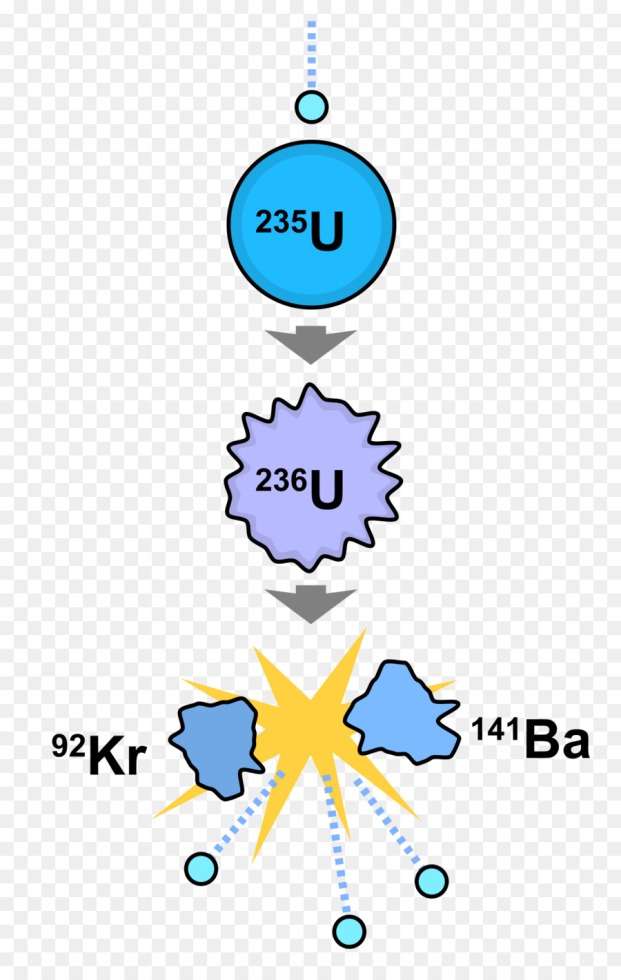
Что такое массовое число ядер элементов нужно знать при составлении реакций радиоактивного распада или ядерных реакций. Например, при делении ядра урана 235U, захватившего один нейтрон 1n, образуются ядра бария 141Ba и криптона 92Kr, а также три свободных нейтрона 1n. При составлении таких реакций пользуются правилом: сумма массовых чисел в правой и левой частях уравнения не меняется. 235+1 = 92+141+3.

